martes, 14 de noviembre de 2017
jueves, 9 de noviembre de 2017
viernes, 3 de noviembre de 2017
SEMANA 35
LA SOLUBILIDAD: Es
la cantidad máxima de soluto que puede disolverse en una cantidad
determinada de solvente a una temperatura previamente establecida.
Generalmente, la solubilidad de una sustancia se expresa en gramos del
soluto por cada 100 gramos de disolvente, por ejemplo, a 20 0C,
la máxima cantidad de cloruro de sodio que se puede disolver en 100
gramos de agua son 36,0 gramos. En la siguiente tabla podemos observar
la solubilidad de NH4NO3(nitrato de amonio), C6H12O6(Glucosa), NaNO3(nitrato de sodio), CH3CO2Na(acetato de sodio), LiCl(cloruro de litio), KBr(bromuro de potasio), NH4Cl(cloruro de amonio), CuSO4(sulfato de cobre II), NaCl(cloruro de sodio) y por último el Ce(SO4)3 (sulfato de cerio III).

puntuación 100%

puntuación 100%
semana 33
luego de observar el vídeo, responde las siguientes preguntas
1. Cuáles son las características de una solución?
2. Cuáles son sus componentes?
3. Mensione otros disolventes diferentes al agua que se pueden utilizar en soluciones
4. Qué es la solubilidad y que factores la afectan?
5. A qué se llaman soluciones empíricas y como se dividen?
6. Que son las soluciones valoradas y cuales se mencionan en el vídeo?
Respuestas
1. es una mezcla homogenea, pueden pasar por papel filtro sin que sus componentes se separen,siempre son liquidas
2.
soluto : es el componente que es disuelto : sal
solvente: es el que disuelve al soluto: agua
3.
tiner
alcohol
gasolina
etanol
4.
solubilidad
La solubilidad es la capacidad de una sustancia o un cuerpo para disolverse al mezclarse con un líquido
los factores que la afectan son la temperatura, presión,polaridad, agitación y efecto del ion común.
5.
soluciones empiricas
Una solución empírica es aquella solución que no posee una concentración determinada.
-solución diluida
-solución concentrada
-solución saturada
-solución sobre saturada
6.Las soluciones valoradas o soluciones estándar son aquellas en las que las medidas de concentración de sus componentes son conocidas y seguidas con precisión. Las medidas de concentración están estandarizadas.
-soluciones porcentuales
-soluciones molares
jueves, 2 de noviembre de 2017
semana 32
Disociación
Disociación en química es un proceso general en el cual complejos, moléculas y/o sales se separan en moléculas más pequeñas, iones o radicales, usualmente de manera reversible. Disociación es lo opuesto de la asociación, síntesis química o a la recombinación.
Cuando un ácido de Brønsted-Lowry se pone en el agua, un enlace covalente entre un átomo electronegativo y un átomo de hidrógeno se rompe por la fisión heterolítica, lo que da un protón y un ion negativo.
El proceso de disociación es frecuentemente confundido con el de descomposición.

Sales
La disociación en sales por solvatación en un solvente como agua significa la separación de los aniones y cationes. La sal puede recuperarse por la evaporación del solvente o por cristalización al reducir la temperatura.
Ácidos
La disociación de los ácidos en una solución significa la liberación de un protón H+, éste es un proceso de equilibrio, esto quiere decir que disociación y la recombinación ocurren al mismo tiempo con la misma velocidad.
miércoles, 1 de noviembre de 2017
semana 31
SOLUCIONES QUÍMICAS:
Las soluciones son sistemas homogéneos formados básicamente por dos componentes. Solvente y Soluto. El segundo se encuentra en menor proporción. La masa total de la solución es la suma de la masa de soluto mas la masa de solvente.
Las soluciones químicas pueden tener cualquier estado físico. Las más comunes son las líquidas, en donde el soluto es un sólido agregado al solvente líquido. Generalmente agua en la mayoría de los ejemplos. También hay soluciones gaseosas, o de gases en líquidos, como el oxígeno en agua. Las aleaciones son un ejemplo de soluciones de sólidos en sólidos.
La capacidad que tiene un soluto de disolverse en un solvente depende mucho de la temperatura y de las propiedades químicas de ambos. Por ejemplo, los solventes polares como el agua y el alcohol, están preparados para disolver a solutos iónicos como la mayoría de los compuestos inorgánicos, sales, óxidos, hidróxidos. Pero no disolverán a sustancias como el aceite. Pero este si podrá disolverse en otros solventes como los solventes orgánicos no polares.
OVA
ALGUNA VEZ TE HAS PREGUNTADO ¿QUÉ CONTIENE EL AIRE?¿QUÉ HAY EN LA LECHE?¿QUÉ FORMA EL BRONCE?¿QUÉ TIENEN LOS LIMPIADORES?¿CUÁL ES LA COMPOSICIÓN DEL AGUA DE MAR? OBSERVA LAS IMÁGENES Y TRATA DE RESPONDER LO PLANTEADO
1.R/ el aire esta formado por oxigeno,nitrógeno,hidrógeno,carbono y otros gases nobles
2.R/ la leche contiene el liquido estraido de la vaca convinado con agua y algunos nutrientes
3.R/ La aleación con mayor sonoridad para fabricar campanas es el denominado metal de campana, que consta de 78 % de cobre y de 22 % de estaño.
4.R/ propiedades quimicas capazes de corroer la suciedad
5.R/ agua y sal


2.R/ la leche contiene el liquido estraido de la vaca convinado con agua y algunos nutrientes
3.R/ La aleación con mayor sonoridad para fabricar campanas es el denominado metal de campana, que consta de 78 % de cobre y de 22 % de estaño.
4.R/ propiedades quimicas capazes de corroer la suciedad
5.R/ agua y sal





lunes, 9 de octubre de 2017
domingo, 8 de octubre de 2017
semana 29
Las Leyes Ponderales:
Las Leyes Ponderales o Gravimétricas son un grupo de Leyes que estudian las reacciones químicas en función de las cantidades de materia de los diferentes elementos que intervienen.
- Ley de Conservación de la Masa (Lavoisier - 1785):
Esta ley afirma que en una reacción química la masa permanece constante. Esto implica que la masa que se consume de los reactivos es la misma que se obtiene de los productos de la reacción.
Otra manera de enunciarla sería: en una reacción química, la materia no se crea ni se destruye sino que se transforma permaneciendo constante.
Solo existe una única excepción a esta ley: las reacciones nucleares en las que parte de la materia se transforma en energía.De esta ley se deduce que el número de átomos permanece constante una reacción.
Ejemplo: sea una reacción en la que reaccionan A y B para dar C. Reaccionan completamente 50 gramos de A y 70 gramos de B para dar C. Calcular la cantidad de C.
Solución: como la materia no se crea ni se destruye sino que se transforma, en este caso se ha transformado toda en C. Por lo tanto la cantidad de C es igual a A + B = 50 + 70 = 120 gramos.
- Ley de Proporciones Constantes o Proporciones definidas (Proust - 1799):
Esta ley afirma que cuando viarias sustancias se unen para formar un compuesto, lo hacen siempre en una relación constante de masa.Esta ley tiene implicaciones importantes. Por ejemplo, a la hora de determinar la fórmula molecular de un compuesto, podemos asegurarnos que los subíncides de cada elemento son fijos.
- Ley de Proporciones Múltiples (Dalton - 1801):
Esta ley afirma que la presión total de una mezcla de gases es igual a la suma de las presiones parciales que ejercen cada uno de los gases que la componen.
Por lo tanto esta ley se puede expresar como:PTotal = p1 + p2 +...+ pn
Donde p1, p2, ..., pn son las presiones parciales de cada uno de los gases de la mezcla.
- Ley de Proporciones Equivalentes (Ritcher - 1792):
Esta ley afirma que la masa de dos elementos diferentes que se combinan con una misma cantidad de un tercero, guardan la misma relación que las masas de los elementos cuando se combinan entre sí.
La Ley de Ritcher permite establecer el peso equivalente o peso equivalente - gramo, que consiste en la cantidad de una sustancia que reaccionará con una cantidad determinada de otra.
En química moderna, el peso equivalente se usa en las reacciones ácido-base y las reacciones redox (reducción-oxidación) para calcular la cantidad de materia que proporciona 1 mol de iones de hidrógeno en el primer caso o de la cantidad de electrones que se consumen en el segundo.
sábado, 7 de octubre de 2017
semana 28
Que es PH

El pH es una medida de acidez o alcalinidad de una disolución. El pH indica la concentración de iones hidrógeno presentes en determinadas disoluciones.
La sigla significa: potencial hidrógeno o potencial de hidrogeniones, Este término fue acuñado por el bioquímico danésS. P. L. Sørensen (1868-1939), quien lo definió en 1909 como el opuesto del logaritmo en base 10 o el logaritmo negativo, de la actividad de los iones hidrógeno.

viernes, 6 de octubre de 2017
semana 27
Métodos de separación de mezclas
SEPARACIÓN MAGNÉTICA
Habrás pensado que la forma más rápida y efectiva de separar el hierro del aluminio es recurrir a un imán (si no tuvieras ninguno podrías improvisarlo, ya que muchos cierres de bolsos y tapas de carcasas protectoras de móvil son imanes). Puesto que el hierro es atraído por el imán pero el aluminio no, habrás solucionado el problema de una manera sencilla.
El método empleado en este caso para separar los componentes de tu mezcla heterogénea recibe el nombre de separación magnética. Solo puede emplearse si uno de ellos presenta propiedades magnéticas (como el hierro) y el resto no.
7.2.DECANTACIÓN
Se emplea para separar líquidos con densidades diferentes y que no se mezclan entre sí (inmiscibles), como el agua y el aceite. En estos casos, se utiliza un embudo de decantación.
FILTRACIÓN
Este método se usa para separar un sólido de un líquido en el cual no se disuelve (no es soluble en él), como la arena en suspensión en el agua. Para ello, se hace pasar la mezcla heterogénea a través de un filtro con un tamaño de poro adecuado (menor que el de las partículas que queremos separar). Habitualmente se emplea un papel de filtro acoplado a un embudo.
7.4.DESTILACIÓN
Se utiliza para separar líquidos solubles entre sí que tienen temperaturas de ebullición muy diferentes, como el agua y el alcohol.
EVAPORACIÓN Y CRISTALIZACIÓN
Se emplea para separar un soluto sólido disuelto en un disolvente líquido, como la sal en el agua. El proceso comienza con la evaporación del disolvente (natural o forzada mediante calefacción) y acaba con la deposición en el fondo del recipiente (generalmente, un cristalizador) del sólido en forma de cristales. Cuanto más lenta sea la evaporación del disolvente, más grandes serán los cristales
semana 26
Partes de la llama

Que es combustible?
Sustancia o materia que al combinarse con oxígeno es capaz de reaccionar desprendiendo calor, especialmente las que se aprovechan para producir calor.h

Que es combustible?
Sustancia o materia que al combinarse con oxígeno es capaz de reaccionar desprendiendo calor, especialmente las que se aprovechan para producir calor.h
semana 25
Laboratorio reacciones químicas
Una reacción química, también llamada cambio químico o fenómeno químico, es todo proceso termodinámico en el cual una o más sustancias (llamadas reactantes o reactivos), se transforman, cambiando su estructura molecular y sus enlaces, en otras sustancias, llamadas productos. Los reactantes pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro de forma natural, o una cinta de magnesio al colocarla en una llama se convierte en óxido de magnesio, como un ejemplo de reacción inducida.
A la representación simbólica de cada una de las reacciones se le denomina ecuación química.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
martes, 26 de septiembre de 2017
semana 24
Estequiometria
es el cálculo de las relaciones cuantitativas entre los reactivos y productos en el transcurso de una reacción química.Estas relaciones se pueden deducir a partir de la teoría atómica, aunque históricamente se enunciaron sin hacer referencia a la composición de la materia, según distintas leyes y principios.
es el cálculo de las relaciones cuantitativas entre los reactivos y productos en el transcurso de una reacción química.Estas relaciones se pueden deducir a partir de la teoría atómica, aunque históricamente se enunciaron sin hacer referencia a la composición de la materia, según distintas leyes y principios.
jueves, 31 de agosto de 2017
semana 23
Reducción-oxidación
Se denomina reacción de reducción-oxidación, de óxido-reducción o, simplemente, reacción redox, a toda reacción química en la que uno o más electrones se transfieren entre los reactivos, provocando un cambio en sus estados de oxidación.
Para que exista una reacción de reducción-oxidación, en el sistema debe haber un elemento que ceda electrones, y otro que los acepte:
- El agente oxidante es aquel elemento químico que tiende a captar esos electrones, quedando con un estado de oxidación inferior al que tenía, es decir, siendo reducido.
- El agente reductor es aquel elemento químico que suministra electrones de su estructura química al medio, aumentando su estado de oxidación, es decir siendo oxidado.2
Cuando un elemento químico reductor cede electrones al medio, se convierte en un elemento oxidado, y la relación que guarda con su precursor queda establecida mediante lo que se llama un «par redox». Análogamente, se dice que, cuando un elemento químico capta electrones del medio, este se convierte en un elemento reducido, e igualmente forma un par redox con su precursor oxidado. Cuando una especie puede oxidarse, y a la vez reducirse, se le denomina anfolito, y al proceso de la oxidación-reducción de esta especie se le llama anfolización.
sábado, 12 de agosto de 2017
semana 22
Ley de la conservación de la materia
Postula que la cantidad de materia antes y después de una transformación es siempre la misma. Es una de las leyes fundamentales en todas las ciencias naturales. Es decir: la materia no se crea ni se destruye, se transforma.
Fue elaborada independientemente por Mijaíl Lomonósov en 1745 y por Antoine Lavoisier en 1785. Esta ley es fundamental para una adecuada comprensión de la química. Está detrás de la descripción habitual de las reacciones químicas mediante la ecuación química. También de los métodos gravimétricos de la química analítica.

Ley de la proporciones múltiples definidas
La ley de las proporciones constantes o ley de las proporciones definidas es una de las leyes estequiométricas enunciada en el año 1795, según la cual cuando se combinan dos o más elementos para dar un determinado compuesto, siempre lo hacen en una relación constante de masas. Fue enunciada por el farmacéutico y químico francés Louis Proust, basándose en experimentos que llevó a cabo a principios del siglo XIX; por lo tanto, también se conoce como la ley de Proust.

Ley de las proporciones múltiples de dalton
Esta ley afirma que cuando dos elementos se combinan para originar distintos compuestos, dada una cantidad fija de uno de ellos, las diferentes cantidades del otro que se combinan con dicha cantidad fija para dar como producto los compuestos, están en relación de números enteros sencillos. Esta fue la última de las leyes ponderales en postularse. Dalton trabajó en un fenómeno del que Proust no se había percatado, y es el hecho de que existen algunos elementos que pueden relacionarse entre sí en distintas proporciones para formar distintos compuestos. Así, por ejemplo, hay dos óxidos de cobre, el CuO y el Cu2O, que tienen un 79,89 % y un 88,82 % de cobre, respectivamente, y que equivalen a 3,973 gramos de cobre por gramo de oxígeno en el primer caso y 7,945 gramos de cobre por gramo de oxígeno en el segundo. La relación entre ambas cantidades es de 1:2 como se expresa actualmente con las fórmulas de los compuestos derivados de la teoría atómica.

Ley de los volúmenes de combinación

Postula que la cantidad de materia antes y después de una transformación es siempre la misma. Es una de las leyes fundamentales en todas las ciencias naturales. Es decir: la materia no se crea ni se destruye, se transforma.
Fue elaborada independientemente por Mijaíl Lomonósov en 1745 y por Antoine Lavoisier en 1785. Esta ley es fundamental para una adecuada comprensión de la química. Está detrás de la descripción habitual de las reacciones químicas mediante la ecuación química. También de los métodos gravimétricos de la química analítica.

Ley de la proporciones múltiples definidas
La ley de las proporciones constantes o ley de las proporciones definidas es una de las leyes estequiométricas enunciada en el año 1795, según la cual cuando se combinan dos o más elementos para dar un determinado compuesto, siempre lo hacen en una relación constante de masas. Fue enunciada por el farmacéutico y químico francés Louis Proust, basándose en experimentos que llevó a cabo a principios del siglo XIX; por lo tanto, también se conoce como la ley de Proust.
Ley de las proporciones múltiples de dalton
Esta ley afirma que cuando dos elementos se combinan para originar distintos compuestos, dada una cantidad fija de uno de ellos, las diferentes cantidades del otro que se combinan con dicha cantidad fija para dar como producto los compuestos, están en relación de números enteros sencillos. Esta fue la última de las leyes ponderales en postularse. Dalton trabajó en un fenómeno del que Proust no se había percatado, y es el hecho de que existen algunos elementos que pueden relacionarse entre sí en distintas proporciones para formar distintos compuestos. Así, por ejemplo, hay dos óxidos de cobre, el CuO y el Cu2O, que tienen un 79,89 % y un 88,82 % de cobre, respectivamente, y que equivalen a 3,973 gramos de cobre por gramo de oxígeno en el primer caso y 7,945 gramos de cobre por gramo de oxígeno en el segundo. La relación entre ambas cantidades es de 1:2 como se expresa actualmente con las fórmulas de los compuestos derivados de la teoría atómica.

Ley de los volúmenes de combinación
Ley de los volúmenes de combinación. Muchos de lo elementos y compuestos son gaseosos, y puesto de que es más sencillo medir un volumen que un peso de gas natural se estudiasen las relaciones de volumen en que los gases se combinan.
Al obtener vapor de agua a partir de los elementos que se había encontrado que un volumen de oxígeno se une con dos volúmenes de hidrógeno formándose dos volúmenes de vapor de agua; todos los volúmenes gaseosos medidos en las mismas condiciones de presión y temperatura.
viernes, 4 de agosto de 2017
martes, 1 de agosto de 2017
viernes, 28 de julio de 2017
Semana 19
estructura de lewis
La estructura de Lewis, también llamada diagrama de punto y raya diagonal, modelo de Lewis, representación de Lewis o fórmula de Lewis, es una representación gráfica que muestra los pares de electrones de enlaces entre los átomos de una molécula y los pares de electrones solitarios que puedan existir. Son representaciones adecuadas y sencillas de iones y compuestos, que facilitan el recuento exacto de electrones y constituyen una base importante, estable y relativa. Esta representación se usa para saber la cantidad de electrones de valencia de un elemento que interactúan con otros o entre su misma especie, formando enlaces ya sea simples, dobles, o triples y después de cada uno de estos se encuentran en cada enlace formado.
La estructura de Lewis, también llamada diagrama de punto y raya diagonal, modelo de Lewis, representación de Lewis o fórmula de Lewis, es una representación gráfica que muestra los pares de electrones de enlaces entre los átomos de una molécula y los pares de electrones solitarios que puedan existir. Son representaciones adecuadas y sencillas de iones y compuestos, que facilitan el recuento exacto de electrones y constituyen una base importante, estable y relativa. Esta representación se usa para saber la cantidad de electrones de valencia de un elemento que interactúan con otros o entre su misma especie, formando enlaces ya sea simples, dobles, o triples y después de cada uno de estos se encuentran en cada enlace formado.
martes, 25 de julio de 2017
semana 18
grupo 6: ácidos e hidracidos
laura villegas
natalia aguirre
susana garcia
grupo 7: sales
daniel tamayo
andres cataño
manuel lopera
andres zapata
laura villegas
natalia aguirre
susana garcia
grupo 7: sales
daniel tamayo
andres cataño
manuel lopera
andres zapata
martes, 18 de julio de 2017
semana 17
expusieron los siguientes grupos.
grupo 4: nomenclatura
Yeison calle correa
Cinthia sanchez celis
William perez marrugo
Mariano perez marrugo
grupo 5: propiedades periodicas
Jorge jimenez
Juan pablo zapata
Esteban gaviria
Andres cardona
Any guzman
grupo 4: nomenclatura
Yeison calle correa
Cinthia sanchez celis
William perez marrugo
Mariano perez marrugo
grupo 5: propiedades periodicas
Jorge jimenez
Juan pablo zapata
Esteban gaviria
Andres cardona
Any guzman
viernes, 14 de julio de 2017
semana 16
expusieron los siguientes grupos.
grupo 3: enlaces químicos
Juan carlos piedrahita angarita
Daniel zapata serna
Santiago avendaño
grupo 3: enlaces químicos
Juan carlos piedrahita angarita
Daniel zapata serna
Santiago avendaño
lunes, 1 de mayo de 2017
semana 15
PROYECTO DE INVESTIGACIÓN
LA TABLA PERIÓDICA
INTEGRANTES:
-Juan José Aristizábal Sarrazola.
-Luis Gustavo Zuñiga Ortega.
-Brahian Camilo Arango Villegas.
-Ricardo Rincón Echeverry.
TEMAS
-Grupos
-Periodos
-Metales y no metales
-Elementos de transición
-Gases nobles
pregunta problematizadora
¿como lograr el entendimiento de la tabla periódica a través de una exposición con ayuda de las TIC?
LA TABLA PERIÓDICA
INTEGRANTES:
-Juan José Aristizábal Sarrazola.
-Luis Gustavo Zuñiga Ortega.
-Brahian Camilo Arango Villegas.
-Ricardo Rincón Echeverry.
TEMAS
-Grupos
-Periodos
-Metales y no metales
-Elementos de transición
-Gases nobles
pregunta problematizadora
¿como lograr el entendimiento de la tabla periódica a través de una exposición con ayuda de las TIC?
martes, 25 de abril de 2017
semana 14
EL DÍA DE LA TIERRA
un día , un pequeño niño estaba sentado a la orilla del mar , este estaba llorando, un hombre se le acerco le pregunto , "por que lloras pequeño", el niño respondió; por que la tierra esta herida
el hombre le pregunto por que decía esto, el niño le mostró por ejemplo un cangrejo muerto en la orilla , el hombre pensó: " es solo un cangrejo muerto", el pequeño le comento que el cangrejo había muerto ahogado por una bolsa, lo cual para el , era una clara muestra de la herida de la tierra, el hombre segia sin entender
el niño lo llevo a un bosque quemado, el pequeño le contó que el solía jugar ahí con sus amigos, asta que el bosque se quemo , por culpa de alguien que dejo una botella de vidrio en medio del bosque, el hombre entendió el mensaje del pequeño , desde entonces , decidió ser un hombre totalmente un protector de la tierra
el niño lo llevo a un bosque quemado, el pequeño le contó que el solía jugar ahí con sus amigos, asta que el bosque se quemo , por culpa de alguien que dejo una botella de vidrio en medio del bosque, el hombre entendió el mensaje del pequeño , desde entonces , decidió ser un hombre totalmente un protector de la tierra
martes, 18 de abril de 2017
semana 13
PRINCIPIO DE EXCLUSIÓN DE PAULI
Dos electrones de un átomo no pueden tener idéntico numero cuántico. este es un ejemplo de de un principio general que se aplica no solo al os electrones sino tambien a otras particulas de spin medio entero.
Principio de multiplicidad (HUND).
Todos los orbitales de una subcapa deben estar ocupados por lo menos por un electron antes de que se le asigne un segundo."al llenar orbitale de igual energia (los tres orbitales P, los 5 D, o los 7 f ) los electrones se distribullen siempre que sea posible, con sus spines paralelos es decir,se parados cuando un orbital contiene unicamente un electron se dice que es desapareado.
martes, 11 de abril de 2017
semana 12
Modelo atómico actual
| |
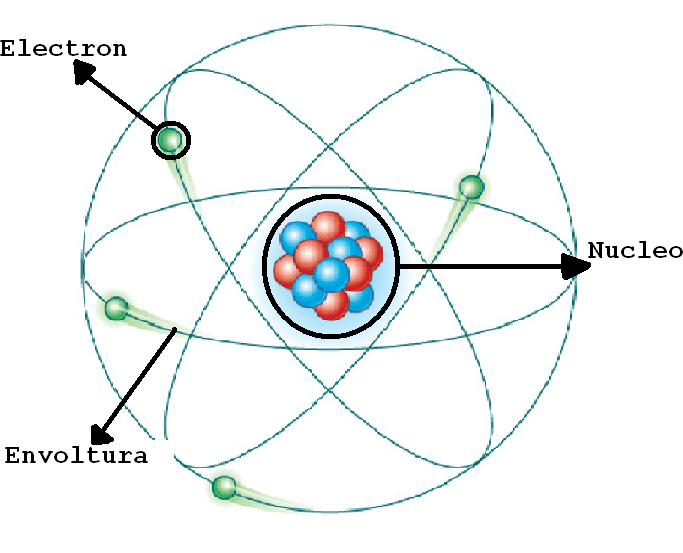
Número cuántico principal (n)
Especifica el nivel energético del orbital, siendo el primer nivel el de menor energía, y se relaciona con la distancia promedio que hay del electrón al núcleo en un determinado orbital. A medida que n aumenta, la probabilidad de encontrar el electrón cerca del núcleo disminuye y la energía del orbital aumenta.
Puede tomar los valores enteros positivos: n= 1, 2, 3, 4, 5, 6, 7.
Número cuántico secundario (ℓ)
También es conocido como el número cuántico del momento angular orbital o número cuántico azimutal y se simboliza como ℓ (L minúscula).
Número Cuántico magnético (mℓ)
Indica la orientación del orbital en el espacio. Puede tomar valores entre:
- ℓ...0...+ℓ
Solo pueden tomar valores enteros que van desde –3 hasta +3, incluyendo el cero.
|
martes, 28 de marzo de 2017
semana #11
segundo periodo
semana 11
VIERNES
COMPORTAMIENTO DUAL DE LA LUZ
la luz tiene un comportamiento dual:a veces se comporta como una partícula y otras como una onda. la luz es una forma de energía electromagnética
Efecto fotoeléctrico
consiste en la emisión de electrones por un material al incidir sobre el una radiación electromagnética
(luz visible o ultravioleta) . aveces se incluyen en el termino otros tipos de relación entre materia y luz:
Desde la antigüedad la humanidad se ha preguntado de que esta formada la materia. En el año 400 A.C el filosofo democrito presento la teoría del átomo, los cuales definía como partículas que no se podían dividir , eran eternos e inmutables, aunque democrito tenia una buena teoría, pasaron 2200 para que su teoría empezara a tomarse en cuenta
MODELO ATÓMICO GRIEGO

MODELO ATÓMICO DE DALTON
dalton expuso su modelo atómico en el año 1808, en el cual dalton definió a los átomos como pequeñas esfera indivisibles e inmutables , iguales ENTRE SI EN CADA ELEMENTO QUÍMICO

EL DESCUBRIMIENTO DEL ELECTRÓN
El 30 de abril 1897, jj thomsom anuncio el descubrimiento del electrón en una conferencia de la royal institucion en londres, el electrón es una partícula mas pequeña presente en todos los átomos lo que demostraba que el átomo no indivisible , thomsom lo descubrió en un laboratorio de la universidad de cambridge

EL MODELO ATÓMICO DE THOMSOM
Esta compuesto por los electrones de carga negativa incrustados en el átomo de carga positiva

DESCUBRIMIENTO DEL PROTON Y EL NÚCLEO
el descubrimiento del proton se le a merita a ernest rutherford , en el año 1918 Rutherford descubrió que cuando se disparan partículas alfa contra un gas de nitrógeno, sus detectores de centelleo muestran los signos de núcleos de hidrógeno. Rutherford determinó que el único sitio del cual podían provenir estos núcleos era del nitrógeno y que por tanto el nitrógeno debía contener núcleos de hidrógeno.
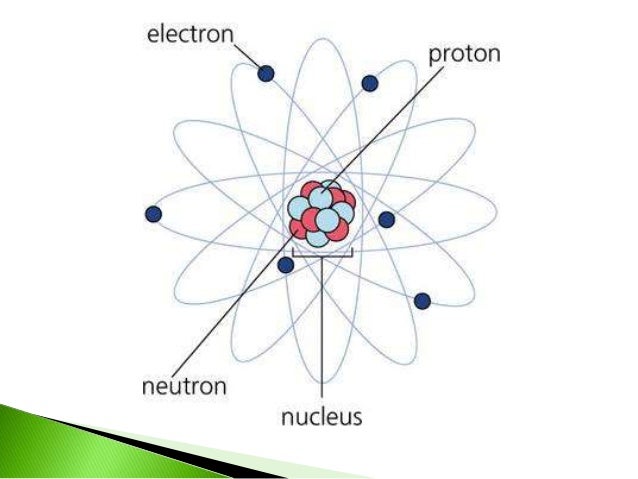
MODELO ATÓMICO DE RUTHERFORD
en el modelo el átomo tiene un pequeño núcleo central, con carga eléctrica al rededor del núcleo giran los electrones en órbitas circulares

MODELO ATÓMICO DE BOHR
borh represento al átomo como un proton en el medio como núcleo , y a su alrededor giraba un electrón dando vueltas de manera circular

QUE ES UN MODELO ATÓMICO
es un representación del átomo que intenta explicar los componentes de este y su forma de una manera gráfica, entendible y completa, la gran mayoría de modelos atómicos son descartados despues de la aparición de nuevas propuestas mas completas
semana 11
VIERNES
COMPORTAMIENTO DUAL DE LA LUZ
la luz tiene un comportamiento dual:a veces se comporta como una partícula y otras como una onda. la luz es una forma de energía electromagnética
Efecto fotoeléctrico
consiste en la emisión de electrones por un material al incidir sobre el una radiación electromagnética
(luz visible o ultravioleta) . aveces se incluyen en el termino otros tipos de relación entre materia y luz:
- Fotoconductividad: Es el aumento de la conductividad eléctrica de la materia o en diodos provocada por la luz. Descubierta por Willoughby Smith en el selenio hacia la mitad del siglo XIX
- -Efecto fotovoltaico: Transformación parcial de la energía lumínica en energía eléctrica. La primera célula solar fue fabricada por Charles Fritts en 1884. Estaba formada por selenio recubierto de una fina capa de oro.
Principio de incertidumbre de Heisenberg
anunciado por W. Heisenberg en 1927, es el echo de que cada partícula lleve consigo una onda , lo cual opone restricciones en la capacidad para determinar al mismo tiempo su posición y velocidad
La partícula de Dios
El bosón de Higgs ( partícula de Dios) constituye el cuanto del campo de Higgs, (la más pequeña excitación posible de este campo). Según el modelo propuesto, no posee espín, carga eléctrica o color, es muy inestable y se desintegra rápidamente: su vida media es del orden del zeptosegundo. En algunas variantes del Modelo estándar puede haber varios bosones de Higgs
MARTES
MODELOS ATÓMICOS:Desde la antigüedad la humanidad se ha preguntado de que esta formada la materia. En el año 400 A.C el filosofo democrito presento la teoría del átomo, los cuales definía como partículas que no se podían dividir , eran eternos e inmutables, aunque democrito tenia una buena teoría, pasaron 2200 para que su teoría empezara a tomarse en cuenta
MODELO ATÓMICO GRIEGO

MODELO ATÓMICO DE DALTON
dalton expuso su modelo atómico en el año 1808, en el cual dalton definió a los átomos como pequeñas esfera indivisibles e inmutables , iguales ENTRE SI EN CADA ELEMENTO QUÍMICO
EL DESCUBRIMIENTO DEL ELECTRÓN
El 30 de abril 1897, jj thomsom anuncio el descubrimiento del electrón en una conferencia de la royal institucion en londres, el electrón es una partícula mas pequeña presente en todos los átomos lo que demostraba que el átomo no indivisible , thomsom lo descubrió en un laboratorio de la universidad de cambridge
EL MODELO ATÓMICO DE THOMSOM
Esta compuesto por los electrones de carga negativa incrustados en el átomo de carga positiva

DESCUBRIMIENTO DEL PROTON Y EL NÚCLEO
el descubrimiento del proton se le a merita a ernest rutherford , en el año 1918 Rutherford descubrió que cuando se disparan partículas alfa contra un gas de nitrógeno, sus detectores de centelleo muestran los signos de núcleos de hidrógeno. Rutherford determinó que el único sitio del cual podían provenir estos núcleos era del nitrógeno y que por tanto el nitrógeno debía contener núcleos de hidrógeno.

MODELO ATÓMICO DE RUTHERFORD
en el modelo el átomo tiene un pequeño núcleo central, con carga eléctrica al rededor del núcleo giran los electrones en órbitas circulares

MODELO ATÓMICO DE BOHR
borh represento al átomo como un proton en el medio como núcleo , y a su alrededor giraba un electrón dando vueltas de manera circular
QUE ES UN MODELO ATÓMICO
es un representación del átomo que intenta explicar los componentes de este y su forma de una manera gráfica, entendible y completa, la gran mayoría de modelos atómicos son descartados despues de la aparición de nuevas propuestas mas completas
martes, 14 de marzo de 2017
martes, 7 de marzo de 2017
SEMANA 8
EN ESTA SEMANA EMPEZAMOS A TRABAJAR CON LAS UNIDADES QUÍMICAS
MOL:1 mol de alguna sustancia es equivalente a 6,O3 × 1023 unidades elementales. La masa de un mol de sustancia, llamada masa molar, es equivalente a la masa atómica o molecular (según se haya considerado un mol de átomos o de moléculas) expresada en gramos
NUMERO DE AVOGADRO:.Es el número de partículas elementales en un mol de una sustancia cualquiera, donde el mol es una de las siete unidades básicas del Sistema Internacional de Unidades .
MOL:1 mol de alguna sustancia es equivalente a 6,O3 × 1023 unidades elementales. La masa de un mol de sustancia, llamada masa molar, es equivalente a la masa atómica o molecular (según se haya considerado un mol de átomos o de moléculas) expresada en gramos
NUMERO DE AVOGADRO:.Es el número de partículas elementales en un mol de una sustancia cualquiera, donde el mol es una de las siete unidades básicas del Sistema Internacional de Unidades .
Suscribirse a:
Comentarios (Atom)





