Modelo atómico actual
| |
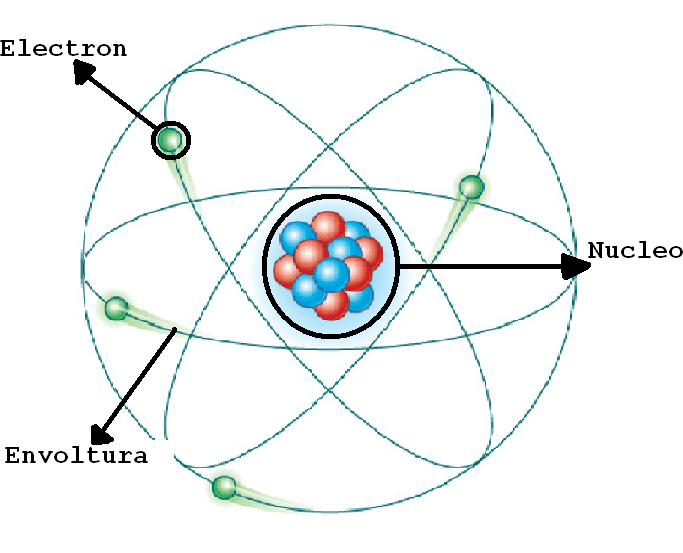
Número cuántico principal (n)
Especifica el nivel energético del orbital, siendo el primer nivel el de menor energía, y se relaciona con la distancia promedio que hay del electrón al núcleo en un determinado orbital. A medida que n aumenta, la probabilidad de encontrar el electrón cerca del núcleo disminuye y la energía del orbital aumenta.
Puede tomar los valores enteros positivos: n= 1, 2, 3, 4, 5, 6, 7.
Número cuántico secundario (ℓ)
También es conocido como el número cuántico del momento angular orbital o número cuántico azimutal y se simboliza como ℓ (L minúscula).
Número Cuántico magnético (mℓ)
Indica la orientación del orbital en el espacio. Puede tomar valores entre:
- ℓ...0...+ℓ
Solo pueden tomar valores enteros que van desde –3 hasta +3, incluyendo el cero.
|
martes, 11 de abril de 2017
semana 12
Suscribirse a:
Comentarios de la entrada (Atom)
No hay comentarios.:
Publicar un comentario